Benutzer-Werkzeuge
Seitenleiste
feature | Synergie als Symbiose
Das Beispiel der Knöllchen-Bakterien: Genossen, Agenten, Kreisläufe
 von Peter Berz
von Peter Berz
An dieser in der Landwirtschaft seit langem bekannten und genutzten Symbiose sind drei Mitspieler, alias Genossen oder Agenten beteiligt: eine Pflanzenfamilie, eine Bakterienart, ein chemisches Element. Die Symbiose agiert in synergetischen Kreisläufen, das ist: in bio-geo-chemischen Prozessen planetarischen Ausmaßes. In der Düngemittelproduktion werden sie Geschichte: Symbiose steht in Konkurrenz zu industriellen Verfahren. Die grundsätzliche Frage nach einer energetischen Zukunft ohne oder einer synergetischen Zukunft mit „companion species“ zeichnet sich ab.
Drei Agenten
Der ERSTE Agent oder Genosse ist eine Pflanzenfamilie. Sie ist wirtschaftlich äußerst bedeutsam. Ihr gehört ein Siebtel aller kultivierten Pflanzen der Erde an: den Hülsenfrüchten, Leguminosen oder Fabaceae, mit der wichtigen Unterfamilie der Schmetterlingsblütler, Faboideae. In dieser Familie leben so berühmte Verwandte wie:
Soja - Bohne - Linse - Klee - Luzerne
Was etwa den Klee betrifft, machte schon Darwin den Witz: „Wer ernährt die britische Armee? Die alten Frauen mit ihren vielen Katzen. Warum? Sie fressen die Mäuse, die Hummelnester zerstören, die den Klee bestäuben, der die Rinder ernährt, von denen unsere glorreiche britische Armee lebt.“ Hier liegt ein Doppeltes vor: einmal die unmittelbare Beziehung von bestäubender Hummel und den lockenden, gelben, in der Junisonne leuchtenden Blüten des Klees als Form einer Symbiose, die Gilles Deleuze und Félix Guattari sogar als „Tier-Werden“ des Klees und ein „Pflanze-Werden“ der Hummel ansprachen;1) und dann der große, vermittelte Kreislauf von Katze Maus Hummel Klee Rind Armee.
Was etwa Soja betrifft: In Dreiviertel aller gekauften und technisch durchstandardisierten Nahrung befindet sich Soja – als Regulator, Emulgator, Geschmacksverstärker, usw.. Soja ist – so der Journalist, Politiker, Betreiber des Gen-ethischen Netzwerks Benny Härlin – der Rohstoff industriell hergestellter Nahrungsmittel. Soja ist ihr „Öl“.
Was etwa die Luzerne betrifft, ist sie ja nur indirekt Nahrung für uns, weil sie vor allem und in großem Maßstab an Tiere, genauer: Wiederkäuer verfüttert wird, unsere Fleischnahrung.
Der ZWEITE Agent oder Genosse ist ein Bakterium. Das Folgende beschränkt sich auf Rhizobium leguminosarum, einen im Jargon symbiotischen Stickstofffixierer. Morphologisch und unter dem Mikroskop sieht das Bakterium stäbchenförmig aus. Es ist beweglich und außerdem aerob, das heißt: in seinem Stoffwechsel kommt die Luft mit ins Spiel. (Außerdem ist Rhizobium leguminosarum „gramnegativ“, zeigt also eine charakteristische, chemische Reaktion seiner „Haut“ alias Zellwand, deren Vorhandensein oder nicht Vorhandensein alle Bakterien in zwei Reiche einteilt – gramnegativ oder grampositiv.)
Der DRITTE Agent oder Genosse trägt den Namen Stickstoffgas oder molekularer Stickstoff, geschrieben als: N2. 80 Prozent der Luft bestehen aus Stickstoffgas. Sein Kennzeichen ist, dass zwei Stickstoffmoleküle – sie sind dreiwertig – miteinander nicht nur eine Einfachbindung (Zeichen: –) oder eine Doppelbindung (Zeichen: = ) eingehen, sondern eine Dreifach-Bindung. Das heißt, dass das Molekül aus einer sehr energiereichen Valenz-Bindung besteht, die nur schwer zu lösen oder zu spalten ist.
Schon hier stellt sich die theoretisch brisante Frage, ob Stickstoffgas im gleichen Sinne ein Agent ist wie eine Hülsenfrucht, also eine Pflanze, oder ein Bakterium, also ein Einzeller. Die eine wie das andere sind Lebewesen. Das Stickstoffgas dagegen ist ein Molekül. Die Frage stellt sich, ob nicht Bruno Latours „Agenten“ genau und nur als diese Grenze und auf dieser Grenze triftig sind: zwischen Molekülen alias Strukturen und Lebewesen alias Agenten? Ja, ob man nicht überhaupt Strukturen und Agenten unterscheiden muss?2)
Vier Prozesse
Die drei symbiotischen Agenten oder Genossen sind im vorliegenden Fall in vier Prozesse eingebaut. Die kleinen Prozesse der Symbiose sind Agenten großer Prozesse, das ist: von geochemischen, biochemischen und vor allem geschichtlichen Kreisläufen. Ganz nach Vladimir Ivanovič Vernadskij.3) Das Zusammenwirken kleiner Symbiosen und großer Kreisläufe ist eine prinzipielle Herausforderung, wenn man über Synergie als Symbiose nachdenkt.
Die vier Prozesse wären:
A. Das Sich-Finden
B. Der Stoffwechsel (Metabolismus als Katabolismus und Anabolismus)
C. Der Kreislauf (Stickstoff-Kreislauf)
D. Konkurrierende industrielle und symbiotische Prozesse
A.
Die im Deutschen so genannten „Knöllchenbakterien“ der Leguminosen sind historisch gesehen in der Landwirtschaft und in der Wissenschaft seit langem bekannt. Ende des 19. und Anfang des 20. Jahrhunderts weiß man bereits viel über sie. Ihre Morphologie ist ausführlich etwa in Paul Kammerers Buch über die „Genossenschaften von Lebewesen“ von 1913 beschrieben (Rhizobium wird hier noch angesprochen als: Bacterium radicicola).4)
- Bakterien und Pflanze finden sich gegenseitig, das ist 1913 noch unklar, entweder zufällig oder weil die Bakterien von den Wurzelhaaren einer Rotkleepflanze angezogen werden. Das Sich-finden als Bedingung aller Synergie ist in der Symbiose zentral. Wie genau geschieht es? Die Frage stellt sich an Kammerers Denken von Zufall und „Gesetz der Serie“, wie Kammerers großes Buch von 1919 heißt (auch wenn die Knöllchenbakterien darin nicht vorkommen, sondern eben im Buch über die „Genossenschaften der Lebewesen“). Aber auch der große, von Kammerer veehrte Symbiose-Theoretiker Pëtr Alekseevič Kropotkin geht von der Frage aus: Wie eigentlich finden sich bei Beginn des Winters die in den endlosen Weiten des Amur verstreuten Dammhirsche, um dann zusammen über den Fluß Richtung Süden zu setzen?5)
 - Nachdem sich Bakterien und Pflanze gefunden haben, dringen die Bakterien ins Wurzel-Haar ein, sie bilden einen Kanal, einen Schlauch und arbeiten sich darin als Schleimfaden vor bis zu den Zellen der Wurzelmitte, um dort eine „schleimige Kolonie“ zu bilden [Abb.: Tafel 8, 1 a].
- Nachdem sich Bakterien und Pflanze gefunden haben, dringen die Bakterien ins Wurzel-Haar ein, sie bilden einen Kanal, einen Schlauch und arbeiten sich darin als Schleimfaden vor bis zu den Zellen der Wurzelmitte, um dort eine „schleimige Kolonie“ zu bilden [Abb.: Tafel 8, 1 a].
- Dann üben sie einen Wachstumsreiz auf die Zellen der Wurzel aus. Die Wurzel verändert ihr Wachstumsverhalten, Kammerer: „wie die Gallen“. Also wie jene von außen, durch Gallwespen, gesteuerte Umlenkung des Pflanzen-Wachstums, durch das die Pflanze eine kleine Kapsel ausbildet, in der sich dann die Gallwespen entwickeln. Bei den Leguminosen ist das Ergebnis: die Wurzelzellen bilden „Knöllchen“.
- In diesen Knöllchen bleiben die einen Bakterien so wie sie sind, die anderen aber verändern sich fundamental. Zunächst morphologisch, in ihrer Form: aus Stäbchen werden gelappte Figuren [Abb.: Tafel 8, 1 e]. Aus den Bakterien werden die so genannten „Bacteroide“.
- Als Bacterioide sind sie in den Knöllchen als Netz oder Fläche verteilt [Abb.: Tafel 8, 1 f]. Kammerers oft analogisches Denken sieht sie „wie die Kiemen von Fischen“.
- Nur, und das ist entscheidend, diese Kiemen nehmen eben keinen Sauerstoff auf, sondern den molekularen Stickstoff der Luft N2.
Dieser ganze Prozess hat also zwei prinzipielle Seiten: Einerseits den Wachstumsreiz durch die Bakterie, das Umlenken des Wachstumsprozesses der Wurzel zur Bildung der Knöllchen (modern: Umprogrammieren). Andererseits bildet sich durch die Aufnahme in die Wurzel die Bakterie selbst um - zum Bakteroid. Erst damit bekommt die Bakterie eine Fähigkeit, die sie frei im Boden lebend nicht hat: sie kann den Stickstoff der Luft N2 fixieren und der Pflanze zur Verfügung stellen. (Andere Bakterien haben auch frei lebend diese Fähigkeit, aber Rhizobium nicht.) Symbiose also heißt hier: strukturelle Veränderung der Partner durch Symbiose. Lamarckistisch gesehen: in der neuen Umgebung, dem neuen Milieu, dem neuen Medium wird das Bakterium ein anderes.
Die Molekularbiologie sagt: die Stickstofffixierung ist im freien Leben „blockiert“ - „Hemmung“ einer Genexpression. Diese Hemmung wird je nach Umgebungsbedingung aufgehoben, nach Jacob/Monods schaltenden Genen wird ein Gen aus- oder angeschaltet. Die Bedingung im Fall der Knöllchenbakterien ist die symbiotische Umgebung der oder in der Leguminosenwurzel.
B.
In den Knöllchen arbeitet der Metabolismus der Bakteroide mit den Kohlenhydraten, das ist: den Zuckern, die die Pflanze zur Verfügung stellt (und mit deren Eiweiß). Das lässt sich, so schon Dr. Kammerer von der Versuchsanstalt im Wiener Prater, experimentell beweisen: man gibt die Bakterien extrazellulär in ein Medium. Erst wenn man Eiweiß und Zucker hinzugibt, spalten sie, in Grenzen effektiv, „molekulären“ (Kammerer) Stickstoff N2.
Die Bakterien spalten N2 und bilden daraus Ammonium NH4+, das sie der Pflanze zur Verfügung stellen. Denn die Pflanze braucht Ammonium zur Synthese von Proteinen und ihren Amino-Säuren. Ergebnis: die Pflanze gedeiht, die Blätter werden größer, mehr Photosynthese findet statt und dadurch bekommen umgekehrt die Bakterien mehr Einweiße und Zucker und gedeihen selbst besser und liefern Ammonium, das - usw.
Ein Enzym macht dabei die Musik: die Nitrogenase. Es ist zweiteilig, ein Dimer, und sehr sauerstoff-anfällig; trickreiche und zahlreiche Maßnahmen verhindern seine zu schnelle Verbindung mit Sauerstoff. Der entscheidende Punkt ist nun, daß die Fixierung des Stickstoffs aus elementarem Stickstoff der Luft N2 äußerst energieaufwändig ist. Chemisch ausgedrückt:
N2 + 8H+ + 8e- + 16 ATP → NH3 + H2 + 16 ADP + 16Pi
Das heißt: Die Fixierung verbraucht 16 Moleküle ATP, Adensosin-Tri-Phosphat, jene „Energiewährung“6) im Metabolismus der Zelle. Diese viele Energie, diese äußerst „hohe ATP Synthese-Rate“,7) bekommt das Bakterium von der Pflanze geliefert, die ATP durch die Glyko-lyse von Zuckern gewinnt. Aber die Bilanz der Glykolyse eines Moleküls Glukose sieht, im Vergleich zur energieaufwändigen N2-Fixierung, mager aus: 2 ATP werden verbraucht, 4 ATP gebildet und damit nur 2 ATP gewonnen. Es muß also viel Zucker glykolysiert werden, um die zur Stickstoffixierung nötige Energie aufzubringen.
EXKURS. Paul Singleton stellt daran anschließend die Frage: Warum haben gerade Bakterien diese Fähigkeit der Stickstofffixierung, aber die Pflanzen nicht? Die Antwort ist selbst symbiosetheoretisch interessant: Die Pflanzenzellen sind durch Endosymbiose entstanden. Doch die stickstofffixierenden Bakterien sind evolutionsgeschichtlich später zu datieren als die Endosymbiose und konnten demnach nicht in die Endosymbiose eingehen. Dem fügt Singelton die sehr denkwürdige Bemerkung des britischen Mikrobiologen John R. Postgate hinzu: Es könne hier aber auch eine „Unzulänglichkeit des Selektionsdrucks als Ursache“ vorliegen.8)
C.
Die Symbiose von Hülsenfrüchten und Knöllchenbakterien steht nicht allein. Sie ist vielmehr Teil eines Kreislaufs: des Stickstoffkreislaufs. Denn wie treibt sich - aufs Ganze gesehen - der Stickstoff in der Welt herum? Im Jargon: Auf welche Weise sind welche Mengen Stickstoff „biologisch fixiert“? Antwort: Stickstoff treibt sich herum und wird fixiert allein durch Bakterien. Mit Vernadskij: Die Biosphäre ist ein bakteriengetriebenes Verkehrssystem, in diesem Fall für den Verkehr von Stickstoff.
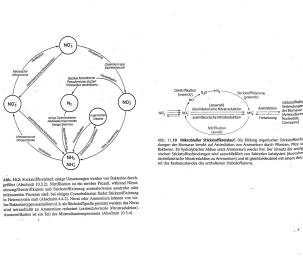 Zunächst existiert Stickstoff eben in der Luft, drei Viertel der Luft sind elementarer Stickstoff N2 mit seiner Dreifachbindung. Dahin kommt er etwa aus Nitrit (NO3) und Nitrat (NO2), in Boden oder Wasser, durch die Aktivität denitrifizierender Bakterien [vgl. Abb.: Kreislauf-Schemata]. Denitrifikation, etwa von Böden, ist für den Menschen meist sehr unerwünscht. Nur in den Prozessen der Abwasserreinigung ist sie sehr erwünscht.9)
Zunächst existiert Stickstoff eben in der Luft, drei Viertel der Luft sind elementarer Stickstoff N2 mit seiner Dreifachbindung. Dahin kommt er etwa aus Nitrit (NO3) und Nitrat (NO2), in Boden oder Wasser, durch die Aktivität denitrifizierender Bakterien [vgl. Abb.: Kreislauf-Schemata]. Denitrifikation, etwa von Böden, ist für den Menschen meist sehr unerwünscht. Nur in den Prozessen der Abwasserreinigung ist sie sehr erwünscht.9)
Pflanzen und Tiere können aber den für alle biosynthetischen Prozesse (Anabolismus), etwa den Aufbau von Aminosäuren, nötigen Stickstoff nicht direkt aus N2 holen. Er ist in dieser Form unverwertbar und kann nur aus Ammonium NH4+ gewonnen werden. Nur einige Bakterienstämme, freilebende oder symbiotische wie Rhizobium, vermögen den molekularen Stickstoff direkt zu verwenden, das ist: Stickstoff aus N2 zu NH4+ zu fixieren.
Erst Ammonium NH4+ können Tiere und Pflanzen zu Amino-Säuren „assimilieren“, also zu Proteinen und Enzymen, das ist: „organischer Materie“. Aus dieser Materie, wenn sie als Abfall ausgeschieden wird oder einfach herumliegt, wird NH4+ dann auch wieder „freigesetzt“: nitrifizierende Bakterien machen daraus wieder Nitrat NO2. Andere Bakterien können auch direkt aus NO2 durch Nitrat-Atmung, also Dissimilation, oder assimilatorische Nitratreduktion NH4+ gewinnen.
Alles das ergibt einen Kreislauf: eben den Stickstoffkreislauf [vgl. Abb.: Kreislauf-Schemata].
D.
Dieser Kreislauf ist nicht nur evolutiv entstanden und Teil der Evolution. Er ist, um auf diese Weise an Kropotkins und Kammerers Genossenschaftwesen anzuschließen, auch geschichtlich, ist Teil der Geschichte. Er steht in einer alten, vielleicht ältesten Kultur-Technik, die im 19. Jahrhundert eine chemische, physikalische, industrielle Technik wird: die Düngung.
In der Landwirtschaft pflanzt man seit langem auf manchen Feldern vor der Aussaat zuerst oder zwischendrin Hülsenfrüchte an, Leguminosen, mit dem einzigen Zweck, sie am Ende als „Gründünger“ wieder in den Boden zu mischen, also unterzupflügen. Damit soll die Stickstofffixierung aus der Luft durch Symbiose von Knöllchenbakterien und Hülsenfrüchten provoziert werden. (Diese alte Kulturtechnik wurde und wird auch in China praktiziert.)
Die zweite, schon Anfang des 20. Jahrhunderts bekannte Methode ist: Man isoliert die Bakterien und stellt eine Substanz aus ihnen her, mit der man dann düngt: das sogenannte „Nitragin“. Gegenwärtig wird Nitragin von der Firma Jost mit Bakterien der Gattung Azotobacter hergestellt und in Flaschen vertrieben, zur Bodendüngung und Saatgutimpfung (www.jost-group.com). Schon Kammerer kennt Nitragin. Es kommt nicht aus der industriellen Chemie, sondern ist ein Bakteriencoctail. Das Problem ist nur, dass die Bakterien sehr spezifisch an ganz bestimmte Pflanzen „gewöhnt“ sind, so die übliche Ausdrucksweise, die nicht nur Kammerers Lamarckismus geschuldet ist. Kammerer zeigt in einem kleinen Versuch mit Bohne, Erbse, Rotklee und Robinie, dass nur Bakterien vom Rotklee den Rotklee auch zum Wachsen bringen [vgl. Abb.: Tafel 8, Fig. 2].10)
Nun ist die Sache aber noch von einer anderen Seite her brisant. Seit nämlich durch Liebigs Agrarchemie überhaupt erst Düngung mit Mineralien, statt organischer Materie denkbar und machbar wurde, also etwa Düngung mit Stickstoff, kommt alles darauf an, geeignete Stickstoffquellen herzustellen, das ist: Ammonium oder Ammoniak NH3. Lange Zeit wird Ammoniak aus Chilesalpeter (Natriumnitrat NaNO3) synthetisiert, das sich in der südamerikanischen Wüste Atacama findet und von dort nach Europa importiert wird. Die Sache hat freilich einen Haken: Chilesalpeter braucht man nicht nur für Düngemittel, sondern auch zur Herstellung von Schießpulver und Sprengstoff. Das geht solange gut wie es genügend Chilesalpeter gibt. Als aber während des Ersten Weltkriegs über Chilesalpeter ein alliiertes Embargo verhängt wird und kein Chilesalpeter, also kein Ammoniak mehr erhältlich ist, heißt das, unter Kriegsbedingungen: entweder verhungern oder nicht mehr schießen, also den Krieg einstellen.
In dieser Lage tritt als Deus ex Katalyse das berühmte Haber-Bosch-Verfahren auf den Plan.11) Die schlichte Formel des Verfahrens steht physikalisch und historisch unter höchstem Druck:
N2 + 3 H2 → 2 NH2
Nach dem Ersten Weltkrieg wird sie zum Kern ganzer Industrien. Um sie zu realisieren, also das N2-Molekül zu spalten und mit dem H2 zu verbinden, ist hoher Druck und hohe Temperatur vonnöten. Steigert man den Druck, kann man die Temperatur senken, damit aber fällt auch die Reaktionsgeschwindigkeit drastisch, die Zeitdauer der Reaktion wird zu lang. Man sucht deshalb nach Katalysatoren, die die „Aktivierungsenergie“ herabsetzen. Man arbeitet zunächst mit teurem Osmium und Ruthenium, bis dann der geniale Chemiker, Philosoph und Chefideologe einer katalytisch-monistischen Wissenschaftsreligion Paul Alwin Mittasch das Eisen als Katalysator einführt.12) Im industriell ausgebauten Verfahren, das vor allem das Problem von Behältern für so hohe Drücke löst, wird dann unter 500° C und einem Druck von 200 bar aus Luft Ammoniak gewonnen: das Ausgangsmaterial für Nitratdünger und Sprengstoff.
Die Düngemittel-Giganten BASF/Wintershall entwickeln daraus nach dem Ersten Weltkrieg, als der Sprengstoffbedarf drastisch sinkt, einen sogenannten Volldünger mit dem Namen NITROPHOSKA, der chemisch Stickstoff, Phosphat, Kalium in einem einzigen Produkt zu einer Ganzheit bindet. Doch das ist nur möglich, weil es die Ammoniaksynthese gibt. Filmisch-propagandistisch unterstützt durch Lehrfilme und schließlich den BASF-Kunst- und -Spielfilm-Film „Das Blumenwunder“ (BASF 1926) wird nun in den 20er und 30er Jahren gedüngt, was das Zeug hält.13) Das desaströse Ergebnis: Überdüngung mit Stickstoff.
In den 30er Jahren machen vor allem finnische Forscher – Arturo Ilmari Virtanen und sein Valio-Labor – eine Feststellung: Überdüngung mit Stickstoff hat schlimme Effekte. Das Winter-Futter für die Kühe, die Silage, in der immer auch Leguminosen sind, stinkt, die Milch stinkt auch und die Butter. Der Grund? Es ist zu viel Stickstoff in dem zur Silage gegorenen Futter und der industriell hergestellte Mineraldünger unterbindet, ja verhindert die symbiotische Stickstofffixierung zwischen Bakterien und Leguminosen. Auch hätte, so die Finnen, die Düngung mit künstlichem Stickstoff schädliche gesundheitliche Effekte und verursache typische Zivilisationskrankheiten an Herz, Gefäßen, ja sogar Krebs.
Der Ausweg, wie die Finnen ihn vorschlagen, ist: Man düngt eben mit Bakterien. Die Energieverschwendung in - trotz Katalyse - Höllentemperatur und Hochdruck nach Haber-Bosch wird zurückgefahren. Denn die Symbiose von stickstoffixierenden Bakterien und Leguminosen macht alles genauer, spezifischer, effektiver und weniger energieaufwändig.14) Die Bakterien setzen 16 ATP-Moleküle dran, die ihnen von ihren Wirten, dem Klee geliefert werden, weil sie den Klee mit Ammonium beliefern - und siehe da: die Milch schmeckt gut und die Butter auch! Die Finnen nennen das in den 30er Jahren, prä-ökologisch, ein „Selbstversorgendes Produktionssystem“, das ist: kalkulierte Verunreinigung des Saatguts mit Knollenbakterien, aus dem Anbau stickstoffabhäniger Gräser wie Weidegras und Taumel-Lolch.15)
Schlußfolgerungen
Und die Moral von der Geschicht'? Symbiose steht - nicht metaphorisch, sondern im historisch Realen - auf den Feldern der Landwirtschaft gegen eine Staatsmaschine namens Industrie-Dünger und chemische Industrie: industrielle versus symbiotische Stickstoff-Fixierung. Damit wäre am Ende eine grundsätzliche Frage aufgeworfen: Lässt sich auf dieser, der Biochemie und Biologie gleich nahen Ebene Synergie auch als companion species denken?16) Denn die symbiotischen Bakterien stehen nicht nur in Genossenschaft, companionship, mit den Fabaceae, sondern sind oder können eine companion species der geschichtlichen Wesen sein, also von uns. Epistemologischer gefragt: Lässt sich companion species als Folge verschachtelter Symbiosen, die Kreisläufe unterhalten, als eine andere, eine synergetische Wissenschaft denken, die ebenso exakt und reich wäre wie die großindustrielle Laborforschung und ihre Technologie des, mit Martin Heidegger gesprochen, Riesenhaften?
Abbildungen aus:
1. Paul Kammerer, Genossenschaften von Lebewesen auf Grund gegenseitiger Vorteile, Stuttgart (Strecker & Schröder) 1913: Tafel 8.
2. Paul Singleton, Einführung in die Bakteriologie (übersetzt von F. Mertens, R. Löscher, engl.: Introduction to bacteria, 2nd ed. 1992), Wiesbaden (Quelle & Meyer) 1995: S. 167, Abb. 10.2. [Abbildung Schema, links]
3. Mikrobiologie (hg. Katharina Munk), Taschenlehrbuch Biologie, Stuttgart (Thieme) 2008, S. 518, Abb. 11.10. [Abbildung Schema, rechts]
Zitierung:
Peter Berz: Synergie als Symbiose: Genossen, Agenten, Kreisläufe. Das Beispiel der Knöllchen-Bakterien, in: Tatjana Petzer (Hg.): SynergieWissen. Interdisziplinäres Forum & Open Access Lexikon, 20.12.2012, http://www.synergiewissen.de